摘要
为构建列线图风险模型以确定支气管哮喘上皮-间质转化的潜在生物标志物,并预测其靶向中药。从GEO数据库下载包含172例哮喘患者和36名健康对照者痰液细胞样本的数据集GSE76262和GSE137268,其中GSE76262用作实验数据集,GSE137268作为独立验证数据集。通过limma R软件包筛选哮喘患者和健康对照者样本的差异表达基因(DEGs),将其与EMT相关基因取交集得到哮喘EMT相关DEGs,并进行功能注释和富集分析。利用Lasso回归分析筛选出核心生物标志物,同时构建列线图预测模型,并通过校准曲线、决策曲线和受试者工作特征曲线评估其诊断效能。利用CIBERSORT探讨哮喘的免疫浸润特性,并进一步分析核心生物标志物与不同免疫细胞之间的相关性。最后,在Coremine Medical数据库预测核心生物标志物靶向中药。共筛选出40个哮喘EMT相关DEGs,其中25个基因上调,15个基因下调。功能富集分析显示,这些DEGs主要参与细胞因子活性、细胞因子介导的信号通路、脂质和动脉硬化、肺纤维化等。CCL22和FKBP5被鉴定为哮喘EMT的核心生物标志物,且其诊断价值有显著意义。CIBERSORT免疫浸润分析显示,哮喘患者和健康对照者样本的免疫浸润特征存在显著差异。在哮喘组样本发现高水平的静息树突状细胞、活化树突状细胞、活化肥大细胞和嗜酸性粒细胞;而在健康对照组发现高水平的初始B细胞、CD8+T细胞、滤泡辅助性T细胞、M0巨噬细胞和M2巨噬细胞。在Coremine Medical数据库预测到小构树皮等48味靶向中药。预测哮喘EMT发生的列线图风险模型具有重要临床意义;CCL22和FKBP5可能是哮喘EMT的关键诊断生物标志物;小构树皮等48味中药可能通过作用于CCL22和FKBP5来干预气道重塑,发挥对哮喘的治疗作用。
Abstract
To construct a nomogram risk model to identify potential biomarkers of epithelial-mesenchymal transition (EMT) in bronchial asthma and predict their targeted traditional Chinese medicine. Two datasets, GSE76262 and GSE137268, including sputum cell samples from 172 asthma patients and 36 healthy controls, are downloaded from the GEO database. GSE76262 is used as the experimental dataset and GSE137268 is used as the independent validation dataset. The differentially expressed genes (DEGs) of samples from asthma patients and healthy controls are screened by limma R software package, and the intersection of these genes and EMT-related genes are obtained as asthma EMT-related DEGs, and functional annotation and enrichment analysis are performed. Lasso regression analysis is used to screen out the core biomarkers, and a nomogram prediction model is constructed. The diagnostic performance is evaluated by calibration curve, decision curve and receiver operating characteristic curve. CIBERSORT is used to explore the characteristics of immune infiltration in asthma, and the correlation between core biomarkers and different immune cells is further analyzed. Finally, core biomarkers targeted traditional Chinese medicine are predicted in the Coremine Medical database. A total of 40 asthma EMT-related DEGs are screened, of which 25 genes are up-regulated and 15 genes are down-regulated. Functional enrichment analysis shows that these DEGs are mainly involved in cytokine activity, cytokine-mediated signaling pathways, lipid and atherosclerosis, pulmonary fibrosis, etc. CCL22 and FKBP5 are identified as the core biomarkers of asthma EMT, and their diagnostic value is significant. CIBERSORT immune infiltration analysis shows significant differences in immune infiltration characteristics between samples from asthma patients and healthy controls. High levels of resting DCS, activated DCS, activated mast cells and eosinophils are found in the asthma group samples. However, high levels of naive B cells, CD8+T cells, follicular helper T cells, M0 macrophages, and M2 macrophages are found in healthy controls. In Coremine Medical database, 48 targeted traditional Chinese medicine, such as broussonetia kazinoki bark, are predicted. The nomogram risk model for predicting EMT of asthma has important clinical significance. CCL22 and FKBP5 may be the key diagnostic biomarkers of EMT in asthma. The 48 traditional Chinese medicine (TCM) such as broussonetia kazinoki bark may intervene in airway remodeling by acting on CCL22 and FKBP5, and play a therapeutic role in asthma.
Keywords
支气管哮喘(简称哮喘)是一种以气道重塑和肺部炎症为特征的慢性炎症疾病,在慢性呼吸道疾病中患病率最高且正以年增长率1.8%的速度持续飙升。据统计,全球至少有3亿人患有哮喘,其中有10%的患者来自中国,该病给社会带来沉重的医疗和经济负担[1-4]。在许多国家,特别是在儿童群体中,哮喘流行率逐渐有所增加,同时死亡率较高[5-6]。哮喘最初也许是可逆的,但由于气道重塑而发展成不可逆状态[7]。上皮-间充质转化(Epithelial-mesenchymal transition,EMT)是动物发育和疾病进展过程中细胞形状变化的基本过程[8]。研究表明,EMT可促进气道重塑[9],哮喘EMT和免疫浸润之间存在复杂的相互作用[10-11]。迄今为止,哮喘EMT发生机制尚不完全明确,以至于限制了哮喘的预防和诊疗。因此目前迫切需要深入了解哮喘EMT与免疫细胞浸润之间的关系,从分子水平鉴定疾病诊疗的生物标志物,有助于为干预哮喘气道重塑进程提供新的思路和策略。
现代医学通过吸入糖皮质激素抑制气道灌注和支气管扩张剂缓解支气管收缩来实现对哮喘的治疗,但其疗效有限且可产生情绪变化、短暂效应、免疫抑制和类固醇对儿童生长的副作用等不良反应[12]。目前中医药治疗哮喘具有一定优势,可有效改善患者生活质量,不良反应较少且依从性较好[13]。“靶向中药”是指针对特定蛋白质或分子靶点的中药药物,具有高度选择性和特异性,能够减少对非靶标的不必要影响[14]。通过挖掘有效靶向中药,可为哮喘的中医临床治疗提供参考和方向,改善中医药防治哮喘的研究现状。近年来,将微阵列技术、生物信息学分析和不同机器学习算法相结合,用于复杂疾病的生物标志物筛选、诊断预测和预后评估已成为各学科热点,计算生物学方法也可为进一步的基础实验设计提供范围和依据[15-16]。
本研究利用生物信息学结合机器学习的方法构建哮喘EMT风险模型,筛选出哮喘EMT特征生物标志物并对其诊断效能进行分析验证,通过模型基因预测靶向中药,同时挖掘疾病相关生物过程、信号通路以及远期并发症,探讨其免疫浸润机制。
1 资料与方法
1.1 数据集选取与注释
芯片数据来源于基因表达综合数据库GEO[17](https://www.ncbi.nlm.nih.gov/gds)中的数据集GSE76262[18]和GSE137268[19],共包含172例哮喘患者和36名健康对照者痰液细胞样本。下载数据集探针矩阵和平台文件,根据平台文件信息,确定探针名称与基因名称的对应关系,将探针矩阵转化为基因矩阵。GSE76262用作实验数据集,GSE137268作为独立验证数据集。
1.2 差异分析与EMT相关DEGs获取
对GSE76262数据集的基因表达矩阵进行差异分析。用较高的阈值可以筛选出更为显著的差异表达基因(Differentially expressed genes,DEGs),但可能会因此错过较小但仍具有生物学意义的变化。考虑到研究问题、流程设计和数据特点,我们选用更具包容性的0.585作为logFC阈值。该阈值表示在两组之间的基因表达至少有1.5倍的差异变化,能够筛选出表达差异相对较小但仍具有生物学意义的DEGs。本研究引用R语言limma软件包,设定|log2FC|>0.585且矫正后P<0.05以获取DEGs,引用ggplot2和pheatmap软件包进行火山图及热图绘制。引用VennDiagram软件包,将DEGs与从上皮-间质转化基因数据库[20](http://www.dbemt.bioinfo-minzhao.org/index.html)下载得到的1 184个EMT相关基因作维恩图,取交集基因为哮喘EMT相关DEGs,引用pheatmap软件包绘制热图。
1.3 EMT相关DEGs功能注释和富集分析
对1.2所得哮喘EMT相关DEGs通过R语言clusterProfiler软件包进行基因本体论(Gene ontology,GO)和京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路富集分析,引用DOSE软件包进行疾病本体论(Disease ontology,DO)富集分析。设定P<0.05为过滤阈值,筛选出具有统计学意义的生物过程(Biological process,BP)、细胞组分(Cellular component,CC)、分子功能(Molecular function,MF)、信号通路以及相关疾病。采用基因集富集分析(Gene set enrichment analysis,GSEA)的方法,以从分子特征数据库[21](https://www.gsea-msigdb.org/gsea/msigdb)下载所得的c5.go.v7.4.symbols.gmt和c2.cp.kegg.v7.4.symbols.gmt基因集作参考,引用limma、org.Hs.eg.db、clusterProfiler和enrichplot软件包对芯片数据集中哮喘样本的基因表达矩阵进行富集分析,获取活跃的生物功能和信号通路。
1.4 Lasso回归分析筛选特征基因与逻辑回归模型构建
通过R语言读取基因表达数据和基因列表文件,再根据基因列表文件,筛选出包含在列表中的基因的表达数据。利用glmnet软件包进行最小绝对值收敛和选择算子(Least absolute shrinkage and selection operator,LASSO)回归分析。将基因表达值作为预测变量,样本组作为响应变量。利用cv.glmnet函数对模型进行交叉验证(Cross-validation,cv),并绘制cv图,确定最佳正则化参数以选择最优模型,再根据Lasso回归的系数,识别具有非零系数的基因,即被选中的特征基因。使用glm函数对筛选所得的特征基因构建初始逻辑回归模型,通过检查模型系数的P值,选择具有显著性的基因(P<0.05)作为新的模型变量。随后基于显著性基因,构建新的逻辑回归模型,并使用步进法进行变量选择。提取新模型的系数、概要统计信息以及置信区间,计算每个基因的Odds Ratio、95%置信区间和P值。最后,通过训练好的最终模型对样本进行预测,计算风险得分。
1.5 构建和评估风险模型
引用R语言rms,rmda和Hmisc软件包,读取临床数据和风险数据以构建逻辑回归模型。使用nomogram函数基于逻辑回归模型创建列线图,展示预测哮喘发生的风险得分与各个风险的关系。使用calibrate函数创建校准曲线,评估模型的性能。计算c-index值,用于评估模型的预测能力。引用limma和pheatmap软件包,提取模型基因表达量,结合样本临床性状数据绘制模型基因热图。
1.6 ROC曲线和决策曲线分析
引用R语言glmnet,pROC和ggsci软件包,对基因和临床性状进行循环,绘制对应的受试者工作特征(Receiver operating characteristic,ROC)曲线,并计算其曲线下面积(area under curve,AUC)值。引用rms和rmda软件包,对“风险得分”、“列线图”和“年龄+性别”三个预测模型进行决策曲线分析(Decision curve analysis,DCA)。
1.7 免疫浸润分析
引用R语言e1071软件包对芯片数据集的校正基因表达矩阵进行免疫细胞浸润分析,过滤免疫浸润结果。用CIBERSORT计算样本基因表达谱中22个免疫细胞的相对比例,调用barplot函数绘制柱状图。通过ggboxplot函数绘制免疫浸润差异箱线图,同时添加两两比较结果。
1.8 模型基因与免疫细胞相关性分析
引用R语言limma,reshape2和ggpubr软件包,读取核心基因在芯片数据集校正基因表达矩阵中的表达量,采用Spearman等级相关分析探讨核心基因表达量与免疫细胞数量之间的相关性并绘制棒棒糖图。
1.9 治疗中药预测
Coremine Medical(https://coremine.com/medical)是一个基于文献的高效、精准数据挖掘服务平台,适用于以基因或蛋白,药物或表型为导向的相关预测以及实验结果的辅助验证。该平台整合了包括美国国家医学图书馆、中国科学院科学研究所、奥斯陆大学和奥斯陆大学医院在内的多个文献数据库资源,被广泛应用于蛋白靶向药物预测。通过将关键蛋白或其相关的信号通路输入到Coremine Medical平台中,我们可以预测相应的治疗方案,包括小分子化合物和中药。中药具有多环节和多靶点作用的生物效应,同一味中药可通过作用于多个不同的靶标来实现多通路调控疾病,发挥协同增效的作用[22]。现将模型基因依次输入Coremine Medical在线平台进行检索,以P<0.05为过滤阈值,评估其潜在疗效、安全性以及可用性,最后筛选整理得到与模型基因相关中药。
1.10 统计学分析
所有统计学计算均采用R 4.2.1及相关软件包完成。qvalue为矫正后的P值,表示P值产生假阳性的概率。相关性采用Spearman等级相关分析。P<0.05为差异具有统计学意义。
2 结果
2.1 EMT相关DEGs识别
筛选出634个哮喘相关DEGs,其中上调基因244个,下调基因390个,见火山图(图1(a)),其中上调基因用红色表示,下调基因以蓝色表示。热图(图1(c))展示了哮喘与健康对照样本中DEGs,颜色由红到蓝,表达量由高到低,分别展示20个上调和下调基因。将1 184个EMT相关基因与634个哮喘相关DEGs作维恩图(图1(b)),交集到40个哮喘EMT相关DEGs,绘制其表达量热图(图1(d)),其中25个基因高表达,15个基因低表达,详情如表1所示。
图1哮喘EMT相关DEGs筛选
Fig.1Screening of asthma-associated DEGs related to EMT
注:(a)DEGs火山图;(b)EMT相关基因与DEGs维恩图;(c)DEGs热图;(d)哮喘EMT相关DEGs热图.
2.2 富集分析结果
GO富集分析筛选出BP条目557个,MF条目26个,没有富集到具有统计学意义的CC条目。由图2(a)可知,BP主要涉及细胞因子介导的信号通路、炎症反应的调节、趋化因子介导的信号通路、趋化因子的反应、趋化因子对细胞的反应等;MF主要包括细胞因子活性、受体配体活性、信号转导受体激活剂活性、细胞因子受体结合、DNA结合转录因子结合等。由图2(b)可知,KEGG富集分析发现相关富集通路主要有脂质和动脉硬化、病毒蛋白与细胞因子及其受体的相互作用、TNF信号通路、趋化因子信号通路、胞质DNA感应通路、流体剪切力与动脉硬化、甲型流感病毒、NOD样受体信号通路、细胞因子-细胞因子受体相互作用、Relaxin信号通路等。DO富集分析得到515种疾病,如图2(c)所示,主要有乙型肝炎、肺纤维化、增殖型糖尿病视网膜病变、糖尿病视网膜病变、视网膜血管疾病、间质性肺疾病、卵巢表皮癌、卵巢癌、细菌感染性疾病、肺炎等。对哮喘样本表达矩阵进行GSEA富集分析,由图2(d)可知,活跃的GO富集条目有αβT细胞活化、细胞因子介导的信号通路、适应性免疫应答的调节、细胞因子受体活性、免疫受体活性。如图2(e)所示,活跃的KEGG富集通路有趋化因子信号通路、细胞因子-细胞因子受体相互作用、JAK-STAT信号通路、自然杀伤细胞介导的细胞毒性、神经活性配体受体相互作用。
2.3 Lasso回归分析筛选特征基因与逻辑回归模型构建
如图3所示,通过Lasso回归分析筛选得到12个特征基因(NEAT1,ERN1,EDN1,LIMA1,CCL22,CXCR4,NME1,ACTL6A,CCL5,SDC2,FKBP5和IL18)。对所得12个特征基因所构建的逻辑回归模型进行变量筛选,过滤出与样本相关性显著的2个特征基因(CCL22和FKBP5)作为模型基因,并构建新的逻辑回归模型,绘制列线图(图4(a))。将性别、年龄、CCL22和FKBP5表达量等相关指标作为列线图模型的预测因子。从中可知,CCL22和FKBP5的高表达以及年龄的增长会增加哮喘患病风险。
表1哮喘EMT相关DEGs
Table1Asthma-associated EMT-related DEGs


图2哮喘EMT相关DEGs富集分析
Fig.2Enrichment analysis of asthma-associated EMT-related DEGs
注:(a)GO富集分析气泡图;(b)KEGG富集分析气泡图;(c)DO富集分析气泡图;(d)活跃的GO富集条目;(e)活跃的KEGG富集通路.

图3Lasso回归分析筛选特征基因
Fig.3Feature gene selection via Lasso regression analysis
注:(a)哮喘中40个EMT相关DEGs的LASSO系数谱;(b)基于log(λ)序列构建的系数剖面图.
2.4 列线图模型验证
在内部实验数据集GSE76262和外部独立数据集GSE137268中验证上述步骤得出的列线图模型。由图4(b)可知,相较于健康对照样本,CCL22和FKBP5在哮喘样本中高表达。校准曲线的C-index值在实验组和验证组中分别为0.868(95%CI:0.782~0.953)和0.817(95%CI:0.706~0.928),校准曲线均趋于理想曲线(图4(c))。决策曲线分析结果(图4(d))显示,无论是在实验组还是验证组,当风险阈值>0.18时,该列线图模型可提供临床净收益,并且列线图模型的临床净收益高于单个变量预测结果。ROC曲线分析结果显示,在实验组和验证组中列线图模型的ROC曲线下面积AUC最大,分别为0.868和0.817(图4(e)),表明该列线图模型具有良好的预测能力,对哮喘患者不良预后的早期识别和及时干预有积极的临床意义。


图4列线图模型验证
Fig.4Model validation of nomogram
注:(a)基于逻辑回归构建模型的列线图;(b)模型基因热图;(c)列线图模型预测能力的校准曲线;(d)列线图模型预测能力的决策曲线;(e)相关变量的ROC曲线.
2.5 免疫浸润分析
通过CIBERSORT算法进行哮喘免疫微环境分析,图5(a)展示了哮喘和健康对照样本中22种免疫细胞的组成分布概况。其中有9种免疫细胞在哮喘和健康对照样本中的浸润差异显著(P<0.05),相较于健康对照组,静息树突状细胞、活化树突状细胞、活化肥大细胞和嗜酸性粒细胞在哮喘样本中上调,初始B细胞、CD8+T细胞、滤泡辅助性T细胞、M0巨噬细胞和M2巨噬细胞则下调,如图5(b)所示。
2.6 模型基因与免疫细胞相关性分析
由图6可知,模型基因CCL22和FKBP5的表达量均与静息树突状细胞数目显著相关,其中CCL22与静息树突状细胞数目呈正相关,FKBP5与静息树突状细胞数目呈负相关。
2.7 潜在治疗中药预测
在Coremine Medical数据库检索模型基因CCL22和FKBP5,以P<0.05作为筛选条件,整理得到潜在治疗中药48味,其中CCL22有小构树皮、合欢花、枳椇子、海藻和皂荚子等30味相关中药,FKBP5有石刁白、枳壳、枳实、香橼和赤芍等18味相关中药(表2)。将上述中药进行归经及性味分析。由图7(a)可知,肝经、肺经、脾经和胃经与支气管哮喘EMT靶向治疗相关性较大,而药物性味主要为苦寒(图7(b))。

图5免疫浸润分析
Fig.5Analysis of immune infiltration
注:(a)免疫细胞浸润比例图;(b)免疫浸润差异箱线图.
3 讨论
目前关于哮喘气道重塑的机制探究颇多,其中EMT被认为是哮喘气道纤维化发生演变的重要作用机制。儿童哮喘症状的严重程度与哮喘持续到成年密切相关且儿童轻中度哮喘气道重塑尚有可逆性[23]。因此,深入探讨哮喘EMT机制的可能生物过程、信号通路和免疫功能,挖掘疾病发生发展过程中潜在的特征生物标志物及其相关治疗中药,及时干预气道重塑,对哮喘患儿的早期正确诊疗尤为重要。


图6模型基因与免疫细胞相关性分析
Fig.6Correlation analysis between model genes and immune cells
注:(a)CCL22与免疫细胞相关性棒棒糖图;(b)FKBP5与免疫细胞相关性棒棒糖图.
C-C基序趋化因子22(C-C motif chemokine22,CCL22)是一类C-C趋化因子,又称巨噬细胞衍生趋化因子[24]。CCR4是CCL22的受体,在Th2细胞中高表达。在过敏性哮喘中,为募集更多的Th2细胞,CCL22与CCR4表达均上调[25]。研究表明,CCL22可诱导天然T细胞向Th2细胞分化,提示CCL22在过敏性哮喘中的致病作用[26]。此外,通过阻断CCR4能够有效减轻气道高反应性,抑制气道嗜酸性粒细胞增加和Th2细胞因子聚集[27]。Zhang等[28]经研究发现M2巨噬细胞分泌多种细胞因子,其中CCL22可以引起骨肉瘤细胞EMT,促进骨肉瘤转移,表明CCL22参与EMT发生过程。FK506结合蛋白5(FK506-binding protein 5,FKBP5)是一种51-kDa蛋白,其C端含有一个与少数蛋白质相互作用的四肽重复基序三单元结构域[29]。皮质类固醇能够有效控制哮喘,FKBP51可调节对皮质类固醇的反应,FKBP5基因多态性与哮喘易感性相关联[30]。另有证据表明,气道菌群失调与哮喘的临床特征有关,并且细菌菌群与特定的气道上皮基因表达谱相关,其中FKBP5基因表达与放线菌相关[31]。D'Angelillo等[32]在其研究中强调了FKBP5在黑色素瘤中促进EMT转分化的功能,该过程受TGF-β的经典调控。以上报道提示CCL22和FKBP5可能是干预哮喘EMT进程的有效靶点,本研究结果与之一致。先前已有关于CCL22和FKBP5这两类生物标志物抑制剂的报道实例,有研究指出黄腐酸能够通过下调CCL22的表达,抑制P38 MAPK和JNK磷酸化来减轻特应性皮炎[33];大麻二酚可以通过抑制小胶质细胞中FKBP5的表达来减轻神经性疼痛[34]。鉴于此,本文通过预测哮喘EMT潜在生物标志物的相关治疗中药,有助于为哮喘的病因病理机制以及临床治疗用药提供新见解。
GO功能富集分析得到的生物功能和过程主要与细胞因子相关。T细胞在分化过程中根据所产生细胞因子的差异分为Th1与Th2细胞,其中Th1细胞主要产生IFN-γ,可活化巨噬细胞,介导细胞免疫;Th2细胞主要产生IL-4和IL-13等细胞因子,可诱导B细胞合成IgE抗体,介导体液免疫,Th1与Th2相互拮抗及促进形成复杂的细胞因子网络共同调节机体的免疫功能[35]。研究表明,哮喘的病理过程与Th1/Th2平衡失调密切相关[36-37]。Jones等[38]研究发现细胞因子TGF-β、IL-6和IL-8能够诱导EMT的发生。TGF-β家族蛋白可以通过调节smad介导的转录因子和下游信号通路来影响细胞的形态和功能,诱导细胞从上皮状态向间质状态的转化,从而促进EMT[39]。KEGG通路富集分析结果中脂质和动脉硬化最为显著。近年来,部分研究发现血脂异常与过敏性疾病有相关性[40]。Jiang等[41]通过脂质组学对比分析发现,哮喘患者体内存在异常的脂质代谢,其中甘油三酯(Triglycerides,TG)含量与哮喘严重程度和血清IgE水平呈正相关,提示升高的TG可能是导致哮喘发展但尚未被认识的病理特征。另有研究指出,EMT通过成纤维细胞的浸润和基质金属蛋白酶的上调在动脉粥样硬化斑块的进展和不稳定中起着至关重要的作用[42-43]。在GSEA富集分析结果中,细胞因子相关生物信号和通路反复出现,进一步肯定了细胞因子在哮喘EMT病理过程中的作用。此外,结果中的Janus激酶/信号转导和转录激活剂(JAK-STAT)信号通路同样受到关注。JAK-STAT通路是一条能够通过生长因子、细胞因子、干扰素和细胞因子信号转导抑制蛋白调节激活的保守通路,并且参与炎症过程[44]。据报道,JAK-STAT通路可能在哮喘治疗中起关键作用[45]。毛细血管扩张共济失调突变体(Ataxia telangiectasia mutated,ATM)是丝氨酸/苏氨酸蛋白激酶磷脂酰肌醇3激酶相关激酶家族的成员,ATM可以通过激活JAK/STAT3通路影响EMT进程[46],由此表明JAK-STAT通路同样与EMT密切相关。
表2模型基因相关中药
Table2Traditional chinese medicines associated with model genes

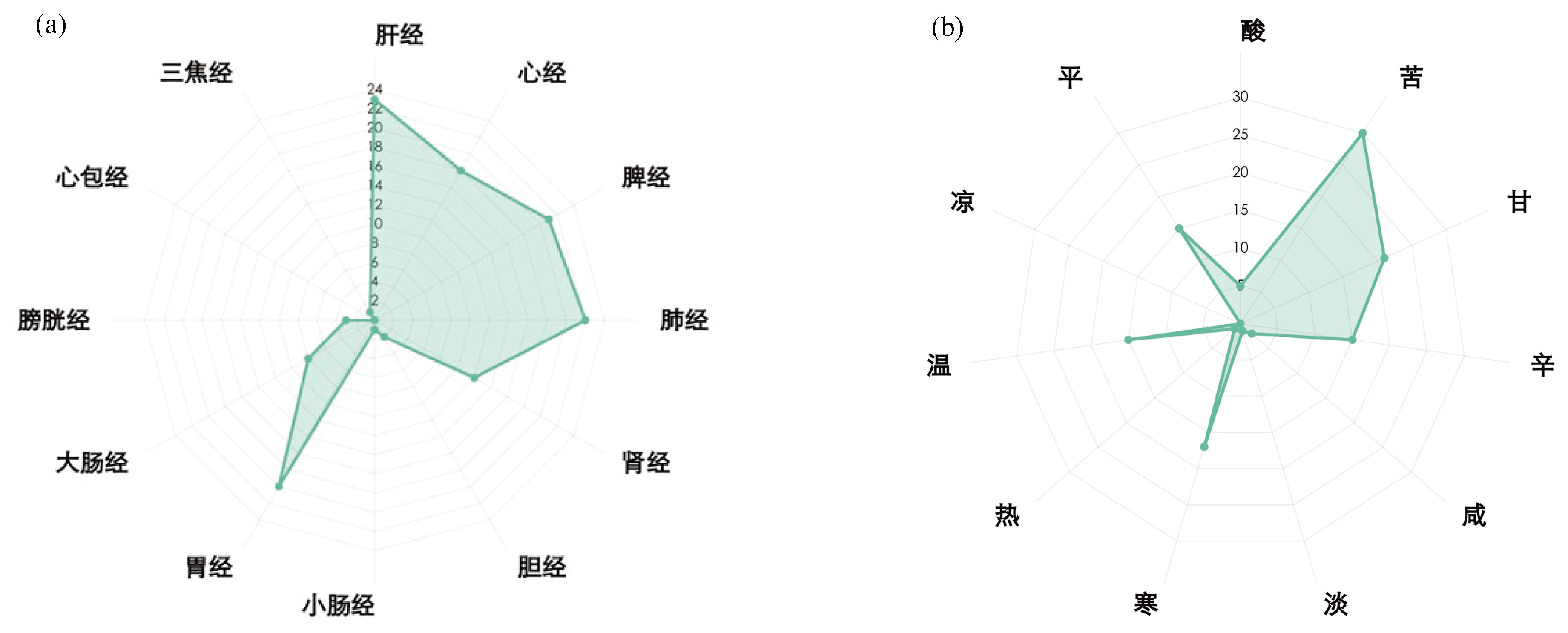
图7相关中药的性味归经
Fig.7Properties, flavors, and meridian tropism of related traditional chinese medicines
注:(a)中药归经雷达图;(b)中药性味雷达图.
通过CIBERSORT算法分析发现,静息树突状细胞、活化树突状细胞、活化肥大细胞、嗜酸性粒细胞、初始B细胞、CD8+T细胞、滤泡辅助性T细胞、M0巨噬细胞和M2巨噬细胞在哮喘和健康对照样本中浸润差异显著。在哮喘的发病机制中,这些免疫细胞可能通过释放炎症介质、激活炎症通路等途径相互作用。树突状细胞可以通过激活记忆性T细胞参与介导抗原特异性免疫应答,并在哮喘慢性气道炎症病理进程中发挥重要作用[47]。肥大细胞在哮喘病理生理学过程中作用关键,当哮喘发生时,气道中肥大细胞的数量增加,并且浸润在各个部位,包括上皮、黏膜下腺和平滑肌束[48]。气道炎症反应是哮喘的主要病理特征,其主要表现为嗜酸性粒细胞(Eosinophils,EOS)的浸润[49]。哮喘发生后,患者血液和痰液中的EOS数量会增多,而且随着哮喘病情的加重,EOS数量也随之增加[50]。据报道,B细胞可以将初始T细胞转化为调节性T细胞,这些T细胞具有治疗炎症性疾病(包括哮喘)动物模型的能力[51]。CD8+T细胞可以通过分泌多种细胞因子来调节哮喘气道炎症[52]。研究发现,外周血滤泡辅助性T细胞CD4+ICOS+和CD4+CXCR5+表达水平与哮喘病情存在负相关关系[53]。巨噬细胞是一异质性群体,具有促炎和抗炎双重作用,其中M2巨噬细胞对过敏性哮喘既有保护作用也有致病作用[25]。本研究结果佐证了现阶段有关哮喘免疫机制的探索,这些免疫细胞类型主要参与免疫调节和炎症反应,而EMT通常受到肿瘤微环境中多种细胞和信号通路的复杂调控。鉴于此,以上免疫细胞对EMT的影响可能主要体现在免疫反应和炎症调节方面,而不是直接地调控EMT的过程。上述免疫细胞或可作为后续哮喘EMT机制研究的关注点和切入点,以期为疾病的发生发展提供更为完善的理论依据,开发更为有效的临床治疗手段。
中医根据病因、病机以及临床表现,将哮喘归类于“哮证”和“喘证”范畴[54]。传统中医认为“痰”是哮喘夙根,“痰”和“瘀”是哮喘主要病理因素,二者贯穿于疾病始终,故治痰治瘀是关键,而肺脾肾三脏亏虚是哮喘发生发展的根本原因,提示哮喘的治疗可从肺脾肾三脏着手[55]。本研究通过在Coremine Medical数据库对哮喘EMT特征基因进行检索,整理得到48味潜在治疗中药,其中麻黄[56]、五味子[57]、皂角刺[58]等中药在哮喘的临床治疗上多有组方应用且疗效显著。通过对以上48味中药进行归经及性味分析,结果发现这些中药主要归属肝、肺、脾和胃经且性寒味苦,由此推测,哮喘EMT或可从肝肺脾肾论治。覃骊兰等[59]认为“肝为起病之源,肺为生病之所”,肝肺生理功能失常是引发哮喘的关键病机,所有的过敏性哮喘都可以“调肝理肺,养血祛风”作为基本原则。刘永平[60]认为脾胃为后天之本,气血生化之源,若脾胃运化水湿功能失调,水液停聚而生痰;痰伏于体内,“伏痰”遇感引触,痰随气升,气因痰阻,相互搏结,壅塞气道,而致痰鸣如吼,气息喘促发为哮喘。不同于传统理论的哮喘从肺脾肾论治,本研究结果提示哮喘EMT可从肝肺脾胃论治,同时从“靶点-中药-归经”的角度揭示了其科学内涵。苦味中药多具有泄、燥、坚的功效。《内经》有云“肺色白,宜食苦”、“肺苦气上逆,急食苦以泻之”。研究发现,人类对苦味的感知由G蛋白偶联受体超家族中的G蛋白偶联苦味受体(Bitter taste receptors,TAS2R)所介导[61],在小鼠哮喘模型中,TAS2R激动剂可减轻活体气道阻力并松弛离体气道平滑肌细胞,且对变应原诱导的气道炎症、重塑和高反应性也有一定的抑制作用[62],提示苦味中药在哮喘治疗中的潜力。
综上所述,预测哮喘EMT发生的列线图风险模型具有重要临床意义,有助于临床对高风险病患的早期筛查和及时干预,降低发病率,改善预后。CCL22和FKBP5可能作为哮喘EMT的关键诊断生物标志物,然而这些生物标志物能否区分不同的内表型尚未清楚。因此,未来有必要进一步研究这些基因对不同内表型的区分效能。此外,哮喘EMT可从肝肺脾胃论治,苦寒中药潜在广阔应用前景,小构树皮等48味中药为中医干预气道重塑的治疗方案提供了更多的选择和参考。




